神経膠腫の治療
神経膠腫について
脳は神経細胞(ニューロン)と神経繊維、神経膠細胞(グリア)から構成されています。
神経膠細胞とは脳の神経細胞の間を埋めて、神経細胞を支持したり神経細胞に栄養を与えたりする役割を担っている細胞群です。
この神経膠細胞から発生する腫瘍が神経膠腫(グリオーマ)で、原発性脳腫瘍の約30%を占めています。
神経膠腫は大きく分けて①星細胞系腫瘍(アストロサイトーマ)、②乏突起膠細胞系腫瘍(オリゴデンドログリオーマ)、③上衣細胞系腫瘍、④脈絡叢系腫瘍に分類されます。
神経膠腫は浸潤性腫瘍で脳にしみ込むように広がり、正常組織との境界は不鮮明です。従って手術で完全に摘出することは基本的に不可能です。
神経膠腫をはじめ、脳腫瘍の診断は世界保健機関(WHO)2016年分類に基づいて行われ、その生物学的悪性度によって大きく4段階(グレード1~4)に分けられています(WHO分類2016)。星細胞系腫瘍のびまん性星細胞腫は、グレード2で、これがさらに悪性化し、グレード3になったものが退形成性星細胞腫です。グレード4の最も悪性な腫瘍は膠芽腫(グリオブラストーマ)です。
これまで、脳腫瘍の分類は、主に顕微鏡で観察した組織学的検査に基づいていましたが、このWHO分類2016では、腫瘍組織の遺伝学的検査がほぼ必須となっています。
神経膠腫では、IDHやp53と呼ばれる遺伝子変異の有無や、染色体1p/19q共欠失(1番染色体短腕と19番染色体長腕が共に欠失している)の有無をもとにさらに細分化されます。
グレード3以上の神経膠腫は手術だけでは再発することが避けられず、手術後に放射線治療や抗がん剤による化学療法が必要となります。神経膠腫は脳に発生する“がん”と考えられています。
神経膠腫の治療ついて
治療は手術、放射線療法、化学療法を組み合わせて行います(集学的治療)。
この中で手術治療は、組織診断を確定し、出来るだけ腫瘍を取り除く意味で最も重要で基本となる治療です。腫瘍は浸潤性で境界がありませんので、全てを取り除くことはできません。しかし症状を悪化させない範囲内で可能な限り多く摘出することが、患者さんの予後改善に寄与します。
当科では、安全に多くの腫瘍を取り除くために、様々な先進技術を駆使しています。
術前MRIにて神経線維の走行を確認(トラクトグラフィー)し、術中にはナビゲーションシステムを用いて、手術操作の部位や重要構造物との関係を確認しながら摘出を行います。
またSEPやMEP、VEPなどの術中神経モニタリング下に手術を行い、神経機能温存と摘出範囲の拡大に努めています。さらに、5-ALA(α-アミノレブリン酸)蛍光標識法を行い、術中に残存腫瘍の有無を確認することにより摘出範囲の拡大が得られています。手術中の病理検査(術中迅速組織診断)にて、グレードが3と4の場合には、ギリアデルという抗癌剤をしみこませたタブレット状の薬剤を脳に直接留置しています。
グレード2の神経膠腫に対する摘出後の治療については学会でも意見が統一されていませんが、グレード3と4の神経膠腫に対しては、摘出術後に局所放射線治療とテモゾロミドという薬剤を使った化学療法を行うことが標準治療となっており、当科でもエビデンスに則った世界水準の治療を行っています。最も治療困難な神経膠芽腫に対しては、2018年から保険診療が認められた新しい治療法である『交流電場腫瘍治療システム(Novo TTF)』も実施可能であります。
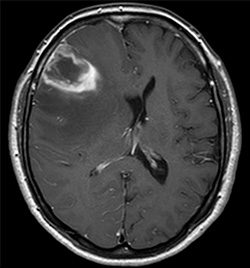
右前頭葉の悪性神経膠腫の術前の造影MRI画像です。
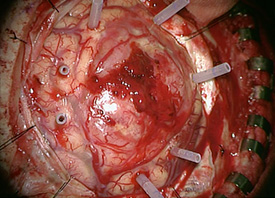 ナビゲーションシステム下でフェンス・ポスト法(あらかじめ摘出範囲を決定しておく)を利用して最大限摘出するように工夫しました。脳に挿入したフェンス・ポスト(透明のチューブ)に沿って腫瘍を摘出していきます。
ナビゲーションシステム下でフェンス・ポスト法(あらかじめ摘出範囲を決定しておく)を利用して最大限摘出するように工夫しました。脳に挿入したフェンス・ポスト(透明のチューブ)に沿って腫瘍を摘出していきます。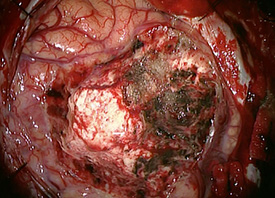 完全に摘出した後です。
完全に摘出した後です。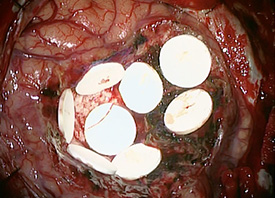 ギリアデルという抗癌剤をしみこませたタブレット状の薬剤(白い円盤)を摘出腔の脳表に直接留置しています。
ギリアデルという抗癌剤をしみこませたタブレット状の薬剤(白い円盤)を摘出腔の脳表に直接留置しています。